GCP机构
| 机构联系方式: | 机构电话: 020-61650039 机构传真: 020-61650039 机构邮箱: nfzxygcp@126.com 接待时间: 周一至周五:上午8:00-12:00,下午14:30-17:30 所在地址: 广东省广州市海珠区石榴岗路13号大院,南方医科大学中西医结合医院27号楼3楼306 机构主任 李爱民 机构副主任 周先举 机构办公室主任 朱志博 18520088084 机构办公室秘书 赖巧 020-61650039 nfzxygcp@126.com 机构质量管理员 黎赛 机构药物管理员 任青 18520088180 机构资料管理员 许希 |
|||||||||||||||||||||
| 伦理委员会联系方式: | 伦理电话: 020-61650040,020-688040 伦理邮箱: nfzxyec@163.com 所在地址: 广州市海珠区石榴岗路13号大院 |
|||||||||||||||||||||
| 科室专业组: | 免疫科 科研助理 赵晓峰 15625065981 科室简介 1、专业科室概况 本科室依托国家中医药管理局重点学科(中医痹病学)、重点专科(中西医结合风湿病)、广东省中医药局重点专科、国家教育部重点学科(中西医结合临床)、广东省“211工程”项目、中国中西医结合学会风湿病专业委员会副主任委员单位、国家食品与药品监督管理局中药新药临床药理基地(中西医风湿病)、国家区域医疗中心中医风湿病(分中心)。 2、病源病种情况 本科室主要病源病种包括类风湿关节炎(RA)、强直性脊柱炎(AS)、系统性红斑狼疮(SLE)、骨关节炎(OA)、痛风(GOUT)、硬皮病(SSc)、结缔组织病(CTD)、银屑病、白塞氏病、皮肌炎等。这些患者主要集中在我科6个优势病种RA、AS、OA、SLE、Gout、SSc中,占比65%以上。 3、设施情况 本专业科室拥有病床32张,其中急救病床2张;有门诊诊室1间、治疗室1间、中医综合治疗室1间、免疫吸附治疗室1间、病房针刀镜手术室1间、关节彩超室1间、四肢关节专用MRI室1间、细胞实验室1间、自身免疫实验室1间、会议室1间、资料室/药物室1间、受试者接待室1间。 4、设备情况 目前,本专业拥有7种抢救设备(呼吸机、除颤仪、吸痰器、心电图、心电监、输液泵、注射泵),4种专科设备(血液灌流机、四肢关节成像诊断系统、关节专用型彩超成像诊断系统、微创针刀镜系统),5种其他设备(电针治疗仪、多功能熏蒸仪、电子脉冲治疗仪、电脑音频药物导入仪、特定电磁波治疗仪)。 5、SOP制定情况 目前,本专业制定了10项制度和62项标准操作规程(应急预案6项、标准规程31项、仪器操作16项、临床技术9项)。 6、研究人员资质、技能和培训情况 本专业现有药物临床试验研究医护人员10名,其中,医生6名,护理人员2名,技师1名,科研助理1名,所有人员均参加了国家级或省级GCP培训。 肾病科 科室简介 1、专业科室情况 本专科依托南方医科大学国家级肾脏病研究整体资源,以中西医结合慢性肾脏病规范化诊疗及肾脏病疑难危急重症诊疗为学科特色,在中西医结合治疗难治性肾病综合征、急慢性肾小球肾炎、慢性肾衰竭、狼疮性肾炎、糖尿病肾病、IgA肾病、膜性肾病、痛风性肾病等方向具有较大优势,并开展血液净化、腹膜透析、肾脏组织活检、动静脉内瘘成形术等肾病专科技术,并根据肾脏穿刺活检病理结合中医辨证论治理论采用中西医结合个体化精准治疗方案。是国家中医药管理局重点学科建设单位、教育部中西医结合临床博士学位授权点、国家重点学科中西医结合临床的主要专业之一、广东省“211工程”三期重点学科建设项目之一。 2、病源病种情况 本专业具有8种常见病种,分别是难治性肾病综合征、急慢性肾小球肾炎、慢性肾衰竭、狼疮性肾炎、糖尿病肾病、IgA肾病、膜性肾病、痛风性肾病等。 3、设施情况 本专业科室拥有病床72张,其中急救病床2张;配备有中医治疗室1间、结肠透析室1间、腹膜透析室1间、受试者接待室1间、资料室1间、药品室1间、抢救室1间。 4、设备情况 目前,本专业拥有5种抢救设备(呼吸机、除颤仪、负压吸引器、心电图机、心电监护仪),4种专科设备(便携式彩超机、连续性肾脏替代治疗机CRRT、血透析机、结肠途径治疗机),5种其他设备(中频治疗仪、超声治疗仪、电脑音频药物导入治疗仪、电子血压计)。 5、SOP制定情况 目前,本专业制定了13项制度和44项标准操作规程(应急预案3项、标准规程31项、仪器操作10项)。 6、研究人员资质、技能和培训情况 本专业现有药物临床试验研究医护人员9名,其中医生5名,护理人员4名,所有人员均参加了国家级或省级GCP培训。 肿瘤科 专业组秘书 宋姗姗 18520088365 - 科室简介 1、专业科室概况 南方医科大学中西医结合医院肿瘤科是中国临床肿瘤学会副会长、广东省中西医结合学会副理事长、广东省抗癌协会副理事长、广东省医学会肿瘤学分会会长、广州抗癌协会理事长单位。 目前,肿瘤科以西医为基础,中医为优势,中西医结合为特色,优势互补,组成了结构完整设施精良、诊疗技术先进、医教研全面发展及团结协作的学科。现展开床位122张,拥有一支结构层次合理、富有朝气的学术和医疗技术队伍。现有主系列医师25人,其中高级职称人员7名,中级职称人员13名,初级职称人员5名;护理团队现有48人,主管护师5人、护师10人,护士33人。科室医护人才结构合理。 目前肿瘤科配备直线加速器、大孔径CT模拟定位机、氩氦刀、射频肿瘤治疗仪、肿瘤微波热疗仪、肿瘤热疗仪、离子植入设备、光动力治疗仪、疼痛创伤治疗仪、超声波治疗仪等设备;可开展常见恶性肿瘤的中西医结合治疗、放化疗综合治疗、肿瘤介入治疗,微创治疗,生物靶向免疫治疗、姑息支持治疗、输液港置入、止痛泵等技术,并开展多种中医特色诊疗技术如穴位敷贴、艾灸、中药熏洗、中医定向透药、耳穴压豆、中药热奄包等,可以系统地对常见恶性肿瘤进行个体化综合治疗、预后评估及毒副反应处理,在肿瘤科常见肿瘤的综合 治疗方面积累了丰富的经验。 2、病源病种情况 本专业现有10种中西医结合优势病种,分别是原发性肺癌(肺癌)、结直肠癌(大肠癌)、淋巴瘤(痰核)、胃癌(胃积)、乳腺癌(乳岩)、原发性肝癌(肝癌)、鼻咽癌(失容)、卵巢癌(积聚)、前列腺癌(癃闭)、食管癌(噎膈);年收治病种超50余种,包括但不限于上述优势病种。 3、设施情况 本专业科室拥有病床122张,其中急救病床4张;有门诊诊室2间、治疗室1间、中医综合治疗室1间、微创手术室1间、DSA手术室1间、会议室1间、资料室/药物室1间、受试者接待室1间。 4、设备情况 目前,本专业拥有7种抢救设备(呼吸机、除颤仪、吸痰器、心电图机、心电监护仪、输液泵、注射泵),8种专科设备(直线加速器、大孔径CT模拟定位机、介入治疗系统、氩氦刀、射频消融治疗仪、放射性离子植入设备、光动力治疗仪、微波热疗仪、6种其他设备(多功能艾灸仪、超声波治疗仪、中药沐足桶、创伤疼痛治疗仪、电子脉冲治疗仪、药物导入仪)。 5、专业制度和SOP制定情况 根据GCP指导原则,肿瘤科专业组建立完善的制度和SOP管理体系,现制定了10项制度和46项标准操作规程(设计规范27项、临床操作技术8项、急救操作规程11项);对项目从方案设计、组织实施、执行、记录、分析、总结和报告等阶段进行规范化,用以药物临床试验全过程,保证临床试验质量,提高临床试验水平。 6、研究人员资质、技能和培训情况 本专业现有药物临床试验研究医护人员14名,其中,医生11名,主要研究者4名,研究者7名,护理人员3名,所有人员均参加了国家级或省级GCP培训,取得GCP证书。 |
|||||||||||||||||||||
| 药物临床试验机构备案信息: | 药物临床试验机构备案信息 (数据来源:NMPA备案平台) 机构基本信息 省份 广东省 备案号 药临床机构备字2020000116 备案时间 2020-03-16 机构名称 南方医科大学中西医结合医院 机构级别 三级 地址 广东省广州市海珠区石榴岗路13号大院 联系人 赖巧 联系电话 15017549166 状态 已备案 备案专业和主要研究者信息
|
CRC政策 SMO合作模式 优先选择有驻点在我院的SMO公司(CRC需有半年以上工作经验)
网址 http://www.nfzxy.com/ywclsy/
一、临床试验组织管理机构情况
1、医院概况
南方医科大学中西医结合医院是南方医科大学(原第一军医大学)第四所直属附属医院。是一所“以西医为基础,中医为特色,中西医结合为优势,肿瘤学科为龙头,多学科协调发展”的综合性教学科研型三级甲等中西医结合医院。2016年规划建设床位为2050张(含肿瘤中心床位600张),现展开床位836张。全院现有员工1070人,正高54人,副高67人,博士生导师39名,硕士生导师58名,博士后合作导师15人,包括有全国优秀教师1名、全国优秀教育工作者1人、广东省教学名师1人、南粤优秀教师1人、广东省“千百十”省级培养对象1人;中央军委保健组专家2名、全国老中医药专家学术经验指导老师3人、全国优秀中医临床人才6人、广东省名中医6名、广东省老中医药专家学术经验指导老师6人。
医院目前拥有1个国家重点学科(中西医结合临床)、6个国家中医药管理局重点学科(中医内科脑病学、中医内科肾病学、中医内科风湿病学、中药药剂学、中药药理学、中西医结合基础)、1个国家中医药管理重点专科(心血管病科)、2个广东省中医药局重点专科(风湿病科和肝胆病科)。

2、机构概况
(1)组织管理机构。设立机构办公室主任、机构办秘书、药物管理员、质控员等岗位,专兼职人员共9人。全面负责各类临床试验项目的管理。机构办公室设在医院27号楼,内设有GCP药房、资料室、会议室等功能区,并配备相应的设备和设施。
(2)建立了临床试验质量管理体系。制订了质量管理的标准操作规程,设质量管理员2名,每个专业组均配备质控员1-3名。
(3)药物临床试验归档资料管理体系。该机构建立了临床试验资料管理制度,设资料管理员1名。
(4)试验药物的管理体系。药物管理人员1名,机构设有药物临床试验专用药房;各专业组均配备带锁专用药柜,专人负责临床试验药物管理,凭研究者专用处方分发药物。
(5)该医院具备开展药物临床试验相关的检测、检验和诊断等相适应的仪器设备,检验科定期参与广东省临检中心组织的临床检验室室间质评。
3、机构人员配备情况
姓名 | 性别 | 学历 | 职称 | 职务 | 分工 |
李爱民 | 男 | 博研 | 主任医师 | 机构主任 | 机构管理 |
周先举 | 男 | 博研 | 研究员 | 机构副主任 | 机构管理 |
朱志博 | 男 | 博研 | 副教授 | 办公室主任 | 主持工作 |
郭小文 | 女 | 硕研 | 主管中药师 | 机构秘书 | 协助管理 |
赖 巧 | 男 | 硕研 | 中药师 | 机构秘书 | 协助管理 |
黎 赛 | 男 | 硕研 | 主管药师 | 质量管理员 | 质量控制 |
晏菲菲 | 女 | 本科 | 主管护师 | 质量管理员 | 质量控制 |
任 青 | 女 | 本科 | 主管中药师 | 药物管理员 | 药物管理 |
许 希 | 女 | 本科 | 主管药师 | 资料管理员 | 资料管理 |
4、构场地建设情况
机构设在我院27号楼,设办公室、药房、资料室、会议室等功能区,并配备直拨电话、传真机等较齐全的设备和设施。

5、机构制度、规范和规程制订情况
根据GCP指导原则,机构建立完善的制度和SOP管理体系,现制定了20项制度、4项规范和34项标准操作规程,对项目从方案设计、组织实施、执行、记录、分析、总结和报告等阶段进行规范化,用以药物临床试验全过程,保证临床试验质量,提高临床试验水平。
6、机构药物临床试验工作流程
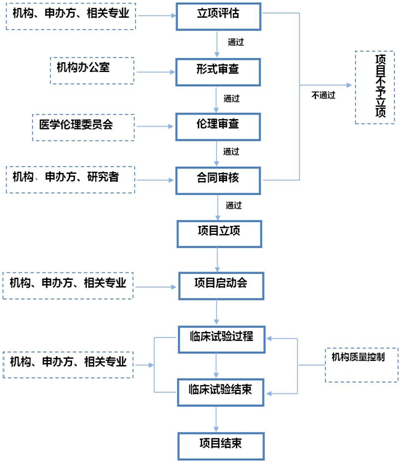
工作流程/常见问题/注意事项
一、立项流程:主要受理项目为Ⅰb、Ⅱ、Ⅲ、Ⅳ期的注册类药物临床试验、药品上市后再评价项目、真实世界研究以及非注册类药物临床试验等。企业项目洽谈应由申办方/CRO 代表直接联系机构办公室,由机构办公室主任负责项目的洽谈,预评估项目可行性。研究者发起的临床试验项目参照非注册类药物临床试验流程执行。

二、合同审核与签署
(1)《临床试验合同书/协议》的模板原则上由机构提供,若申办方有特殊要求的,可接受申办方合同模板。
(2)合同预算应包括但不限于:检验检查费、病例观察费、受试者补助、药物管理费、质量管理费、机构管理费以及相应的税费等。
(3)《临床试验合同书/协议》原则上由机构与申办方直接签订。若申办方委托CRO签订者,则须附《申办方承诺函》,明确各方职责。(双方协议或三方协议均可)
(4)时限:约两周(项目立项后可同步进行)
三、人类遗传备案
(1)适用范围:适用于我院作为参研单位,凡涉及中国人类遗传资源采集、保藏、出境、国际合作科学研究、国际合作临床试验、信息对外提供或开放使用、重要遗传家系和特定地区人类遗传资源等项目,均需完成人类遗传资源信息备案工作。
(2)按《人类遗传审核备案表》附件清单内容递交,应包括但不限于①关于“人类遗传资源采集、收集、买卖、出口、出境审批手续承诺书;②人类遗传资源采集、收集、买卖、出口、出境审批申请书;③第三方实验室承诺书;④组长单位伦理委员会批件等;相关申请表格可邮件向机构索取。
四、项目启动
(1)人员要求
监查员(CRA)
①启动前指定项目的监查员,申办方需保证监查员资质符合法规要求。
②监查员提供以下资料至机构办公室备案:监查员委托书、个人简历、身份证复印件、GCP 培训证书,上述材料均需盖公章。
③监查员提交项目《监查计划》,并签署《监查员告知书》。
2、临床研究协调员(CRC)
①在我院机构开展的临床试验项目,均须配备临床研究协调员(CRC)。
②有三个月以上的临床研究协调经验。
③参加项目启动会培训,PI授权后方可开展工作。
④工作范围:非医学性判断的相关事务性工作。
(2)项目资料、试验药物要求
①项目文件资料
包括但不限于试验方案、研究者手册、CRF 表、招募广告、知情同意书、受试者筛选表与入选表、受试者鉴认代码表等交至专业组资料管理员处,完成资料交接工作。
②试验药物交接
由申办方/CRO、机构药物管理员双方共同完成试验药物交接,填写《临床试验药物出入库登记表》;将药物交给 GCP 药房统一管理(药物管理员:任青,电话:18520088180)。
试验用药物运输过程需保存湿温度记录,常温与室温储存的药物同样需要运输过程的温湿度记录。若有特殊储存条件的药物建议采用冷链或特殊方式运送。
(3)项目启动会召开
①场地
申办方/CRO 需提前至少 5 个工作日与主要研究者、机构办公室确定启动会事宜,包括时间、地点、参加人员等。
②参加人员
参加启动会的人员应包括申办方/CRO人员、研究者、研究护士、专业组秘书、专业组质量管理员、专业组资料管理员、机构质量管理员、机构药物管理员及其他人员。
③资料准备:
应包括但不限于临床试验方案、研究者手册、培训 PPT;PPT 内容应包括药物简介及研究背景、试验步骤、入排标准、知情同意过程、CRF 表的填写、评价方法、AE/SAE 的报告、试验的注意事项、监查计划。
④人员授权:
由主要研究者明确试验分工,并对试验相关人员进行授权,包括但不限于研究者、研究护士、机构药物管理员、临床研究协调员(CRC)。
⑤机构信息系统填报:
由临床研究协调员(CRC)将临床试验项目信息载入信息系统,并让机构办公室主任授权研究人员登录账号,用于检验单据开具和试验用药发放。
⑥会后资料整理、提交:
包括但不限于人员授权分工表、启动会签到表、启动会会议纪要、培训PPT、会议照片以及相关表格等复印件提交至机构办公室备案。原件存于项目组资料文件夹,后续归档统一递交至机构资料室。
